
ББК54.1
фический субаортальный стеноз
параты
кардия
атит
легких
креатография
Чл.-корр. РАМН, заслуженный деятель науки РФ, проф. В. И. Маколкин
Д-р мед.наук, проф. СИ. Овчаренко
- --
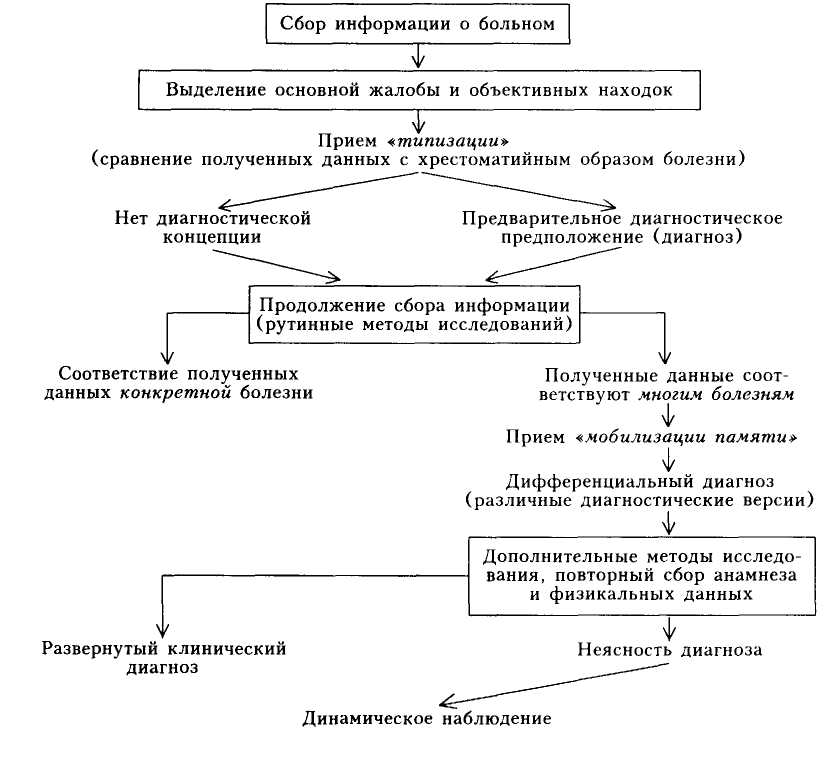
Беседа с больным (изучение жалоб, анамнеза болезни, анамнеза
жизни).- -- Непосредственное (физическое) обследование больного: осмотр,
пальпация, перкуссия, аускультация.- -- Данные лабораторно-инструментальных методов исследования
(так называемые рутинные методы, производимые всем больным, и иссле
дования по специальным показаниям, обусловленным особенностями кли
нической картины болезни у больного). - -- Непосредственное (физическое) обследование больного: осмотр,
таковым при такой-то нозологической форме; иначе говоря, после первого
этапа диагностического поиска диагностическая концепция является впол
не определенной и на остальных этапах ее надо лишь подтвердить, а
также детализировать отдельные проявления болезни;
лезнях, в связи с чем после I этапа диагностического поиска можно лишь
наметить круг болезней, в который входит заболевание данного пациента
(речь идет о так называемом методе дифференциальной диагностики,
о чем более подробно с приведением конкретных ситуаций будет сказа
но позже). Диагноз в данном случае может быть поставлен лишь после
получения информации на II или даже III этапе диагностического по
иска;
определенного заболевания. Это так называемые общие симптомы (сла
бость, утомляемость, потеря массы тела, субфебрилитет и пр.). При такой
ситуации сделать какие-либо заключения после I этапа не представляется
возможным.
больным.
уточнения диагноза (дополнительные исследования).
- --
общий анализ крови,
- -- общий анализ мочи,
- -- общий анализ кала,
- -- биохимический анализ крови (общий белок, сахар, холестерин,
билирубин, креатинин),- -- реакция Вассермана,
- -- ЭКГ,
- -- рентгенологическое исследование органов грудной клетки.
- --
- -- общий анализ мочи,
кретной диагностической ситуации. Так, у легочного больного к
обязательным клиническим анализам добавляется общий анализ
мокроты, при необходимости микробиологический анализ (посев)
мокроты, исследование чувствительности микрофлоры к антибиоти
кам. Определяется перечень необходимых биохимических, фер
ментных, иммунологических и других исследований, инструмен
тальные манипуляции (бронхоскопия, функция внешнего дыхания,
компьютерная томография, бронхоальвеолярный лаваж).
тверждения тех или иных диагностических предположений. Всем
женщинам, находящимся на обследовании в стационаре, необходи
ма консультация гинеколога.
пах диагностического поиска, полностью подтверждается;
пов реализуется в четкий диагноз;
хирургическое вмешательство (например, пробная лапаротомия) или дли
тельное динамическое наблюдение за больным с обязательным выполнени
ем ряда лабораторно-инструментальных исследований.
- --
Насколько получаемые сведения, сообщаемые больным, являются
свидетельством существования патологического процесса, т.е. отличаются
от нормы.- -- Что означают полученные физикальные данные (например, смеще
ние левой границы относительной тупости кнаружи от левой грудинно-
ключичной линии; сухие свистящие хрипы; приступы сжимающих болей
за грудиной, возникающие при физической нагрузке и пр.).- -- Свидетельствуют ли полученные лабораторно-инструментальные
данные о наличии какого-либо патологического процесса. Далее следует с а-
мое важное в диагностическом процессе: полученную информацию
сравнивают с так называемыми эталонами болезней, их "образами", кото
рые хранятся в памяти врача, учебнике и медицинской литературе. - -- Что означают полученные физикальные данные (например, смеще
- --
Вначале выявляют доминирующие симптомы, т.е. любые при
знаки болезни, доступные определению. При этом не имеет значения,
какой источник информации используется.- -- Далее осуществляется "сложение" выявленных симптомов в
синдромы. - -- Далее осуществляется "сложение" выявленных симптомов в
синдромы, оказывается возможным локализовать патологический
процесс в какой-либо системе организма или отдельно взятом органе (на
пример, в печени, сердечно-сосудистой системе, почке, системе кроветво
рения и пр.), при этом симптом лишь "указывает", где локализован пато
логический процесс и крайне редко говорит о существе патологического
процесса; синдром позволяет определить (выяснить) патологоанатомичес-
кую и патофизиологическую сущность патологического процесса (напри
мер, воспаление на иммунной или бактериальной основе, расстройства
кровообращения в той или иной сосудистой области, бронхиальную об
струкцию и пр.). Нередко у одного больного имеется несколько синдро
мов (например, синдром дыхательной недостаточности, бронхиальной
обструкции, легочной гипертензии). Выделение ведущего (ведущих) син
дромов уже существенно приближает нас к нозологической диа
гностике, так как тот или иной синдром (или группа синдромов) свойст
вен весьма ограниченному кругу болезней.
Схема 1. Симптомы--синдромы--болезнь
|
|
|
|
|
|
|
|
|
|
|
Болезнь (болезни)
11
- --
"Образ" болезни, выявленный у исследуемого пациента полно
стью и совершенно безапелляционно соответствует какому-то опре
деленному (одному) заболеванию. Это так называемый пря
мой диагноз, так бывает не слишком часто. Более характерна другая си
туация.- -- "Образ" болезни "похож" на два, три заболевания и более. Тогда
очерчивается "круг" заболеваний, которые надо дифференциро
вать, т.е. в данной ситуации мы пользуемся методом дифференци
альной диагностики (проводя анализ полученной информации,
смотрим, какому из дифференцируемых заболеваний информация соот
ветствует в наибольшей степени). Для постановки диагноза часто нужна
дополнительная информация (получаемая с помощью использованных
ранее методов исследования) или же необходимо динамическое
наблюдение за больным, во время которого симптоматика становит
ся более отчетливой. Длительность такого наблюдения различна -- от не
скольких дней до нескольких месяцев (реже -- несколько лет). Так быва
ет обычно в начальном периоде ("дебюте") болезни. - -- "Образ" болезни "похож" на два, три заболевания и более. Тогда
- --
этиологию (если она известна);
- -- клинический (клинико-морфологический) вариант болезни;
- -- фазу (ремиссия -- обострение);
- -- стадию течения (начальная, развернутая, терминальная);
- -- отдельные наиболее выраженные синдромы (результат вовлечения
в патологический процесс различных органов и систем);- -- осложнения.
- -- клинический (клинико-морфологический) вариант болезни;
- --
Лекарственная терапия, которая подразделяется на терапию в "пол
ной дозе" (когда имеется "дебют" болезни, ее развернутая стадия или обо
стрение) и поддерживающую терапию (лекарства можно давать в меньшей
дозе, но это необязательное условие, так как в ряде случаев дозы лекарст
венных препаратов не уменьшаются при поддерживающей терапии).- -- Физиотерапевтическое лечение.
- -- Санаторно-курортное лечение.
- -- Физиотерапевтическое лечение.
13
Глава I
Содержание
- --
Пневмония при иммунодефицитных состояниях.
- -- Атипично протекающие пневмонии.
15
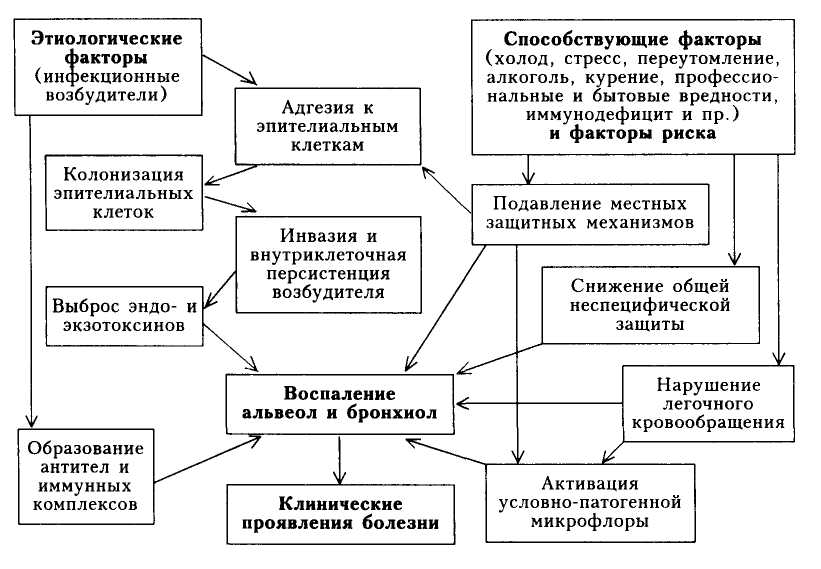
17
шечные боли, одышка, сердцебиение, бледность, снижение аппетита).
повышение температуры тела, изменение острофазовых показате
лей крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево,
увеличение СОЭ, уровня фибриногена, аг-глобулинов, появление
С-реактивного белка -- СРБ).